http://www.ras.ru/news/shownews.aspx?id=4ce5b0da-e8f1-4819-9ad2-b2841ce0c5ba&print=1
© 2024 Российская академия наук
Международная группа ученых, в которую входит
представитель ФИЦ биотехнологии РАН, ИОГЕН и МФТИ, разработала новый, более
надежный метод для изучения контактов РНК с ДНК в ядре клеток. Метод поможет
определить роль РНК в регуляции работы генов, что в будущем
может быть важно, например, для лечения различных
заболеваний Статья об исследовании опубликована в Nature Communication. Работа была поддержана Российским научным фондом (РНФ).
РНК и активность генов
Ранее считалось,
что РНК — это лишь промежуточная стадия между ДНК и белком (рисунок 1а). Но
когда научный мир начал описывать работу генома, оказалось, что далеко не все
участки ДНК кодируют РНК. Более того, даже те, с которых считывается РНК, не
обязательно кодируют белки. Функция большинства некодирующих РНК до сих пор
неочевидна. В разных типах клеток должны работать разные гены и синтезироваться
разные белки: в клетке мозга — одни, в клетке крови — другие. Это значит, что
существуют факторы, которые влияют на активность генов. Теперь ученые начали
понимать, что некодирующие РНК также являются одним из этих факторов.
Известно, что
длинные некодирующие РНК взаимодействуют с хроматином — веществом, которое
представляет собой молекулу ДНК, плотно упакованную с помощью белков (рисунок
1б). Хроматин может менять свою структуру: разворачиваться и сворачиваться, открывая
гены для считывания или, наоборот, закрывая их. Если некодирующие РНК
связываются с определенными участками хроматина, они могут влиять на его
структуру и таким образом регулировать активность этих участков. Чтобы
понимать, как регулируется активность генов и как это влияет на специализацию
клетки, необходимо знать, какие некодирующие РНК с какими участками
связываются.
Как это работает
Есть несколько
методов, которые позволяют определять места, где взаимодействуют РНК и
хроматин. Однако из-за ряда ограничений они пропускают много взаимодействий, к
тому же некоторые из них требуют для анализа большого количества материала или
разрушения клетки. Авторы работы разработали новый метод, который не разрушает
клетку до закрепления контактов РНК и хроматина и показывает более высокую
точность, — они назвали его RADICL-seq.
В ядре клетки
большинство РНК связаны с хроматином: РНК закрепляется в белках, которые
связывают ДНК. Метод RADICL-seq заключается в следующем. В ядро добавляется
фермент, который делает разрывы на ДНК и оставляет свободные концы, пригодные к
сшивке. Также добавляется фермент, который разрушает свободные РНК и тем самым
повышает точность определения контактов. Потом добавляют молекулу, у которой
один конец — одноцепочечный и связывается с РНК, а второй — двухцепочечный и
связывается с расположенной рядом ДНК (рисунок 2а). Таким образом, эта молекула
служит мостиком, скрепляющим РНК и ДНК. Дальше удаляют белки, достраивают
вторую цепочку и получившийся ДНК-комплекс готовят к секвенированию (рисунок
2b), где определяют последовательности связанных РНК и ДНК.
Раскодировать некодирующее
Ученые проверили
метод RADICL-seq в действии. По сравнению с другими методами, он показал более
высокую точность определения хроматин-РНК-взаимодействий.
Благодаря
высокому разрешению метода авторам удалось найти новые контакты не только
некодирующих, но и кодирующих РНК с хроматином, включая те, которые расположены
вдали от мест, где данная РНК считывается. Также они показали на клетках мыши,
что метод подходит для изучения специфики взаимодействий в разных типах клеток.
Они взяли две некодирующие РНК (одна из них, возможно, связана с шизофренией) и
построили карту их взаимодействий с геномом в двух типах клеток: эмбриональных
стволовых и предшественников олигодендроцитов (нейроглиальных клеток). Карты
получились характерными для данных типов клеток и РНК (рисунок 3).
Исследование подтвердило
важную роль длинных некодирующих РНК в регуляции участков генома, удаленных от
мест считывания этих РНК. Гибкость метода RADICL-seq позволяет получить
дополнительную биологическую информацию при внесении изменений в эксперимент. В
частности, дает возможность обнаружить взаимодействия РНК-ДНК, не
опосредованные белками хроматина. Наличие таких контактов указывает на роль в
регуляции экспрессии генов не только канонических взаимодействий (таких как
РНК-ДНК двойные спирали), но и неканонических (триплексов РНК-ДНК-), а также на
значение некодирующих РНК в нацеливании белковых комплексов в конкретные места
генома.
«Мы планируем дальше
исследовать, как РНК участвует в регуляции экспрессии генов, архитектуры
хроматина и, в конечном счете, на идентичность клеток. Вполне возможно, что в
будущем с помощью этих некодирующих РНК можно будет контролировать активность
конкретных генов, что важно, например, для лечения различных заболеваний», —
прокомментировала Юлия Медведева, заведующая группой регуляторной
транскриптомики и эпигеномики ФИЦ биотехнологии РАН и заведующая лабораторией
биоинформатики клеточных технологий МФТИ, руководитель проекта по гранту РНФ.
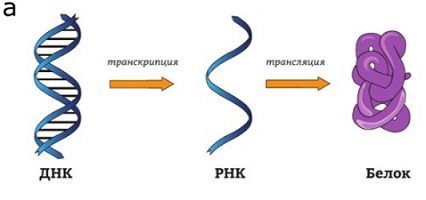
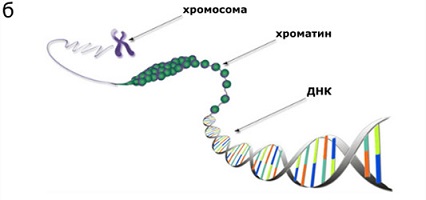
Рисунок 1. а)
Реализация генов: с ДНК считывается РНК, а с РНК — белок.
б) В ядре клетки
молекула ДНК упакована с помощью специальных белков в хроматин, из которого и
состоит хромосома.
Источники: Таблица
генетического кода; Wiring
Diagram Database, Diagram Of Chromatin
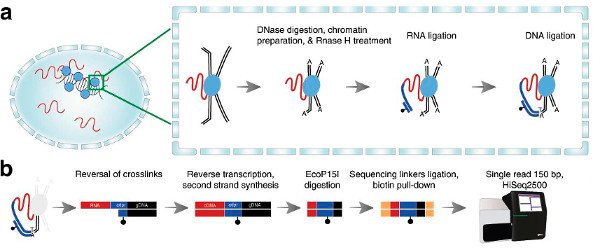
Рисунок 2. а)
Реакции, производимые в ядре клетки. Красным показана РНК, черным — ДНК,
голубым — белки, синим — связующая молекула. Черная точка — молекула,
позволяющая «выцепить» комплекс из раствора. Пояснения даны в тексте.
b)
Реакции, производимые в растворе: 1) удаляются белки, 2) достраивается вторая
цепь, 3) обрезается до определяемого размера, 4) присоединяются
последовательности для распознавания и 5) производится секвенирование.
Источник: Nature Communication
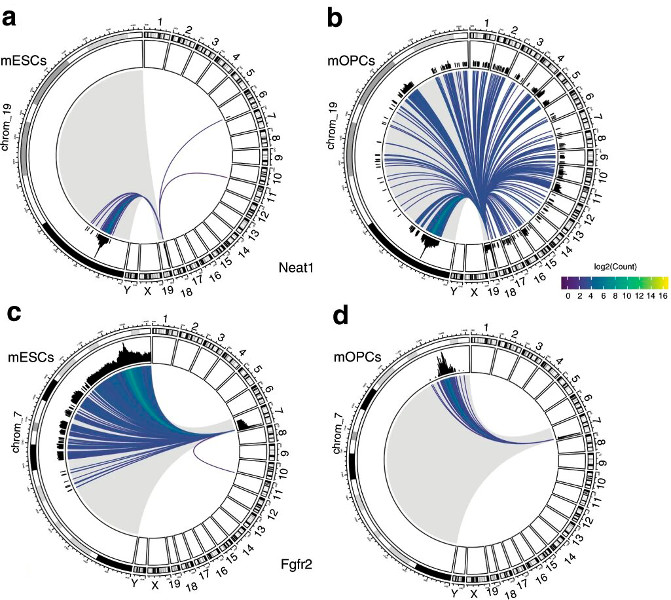
Рисунок 3.
Диаграммы, изображающие взаимодействия некодирующих РНК: Neat1 (a, b) и Fgfr2
(c, d) в эмбриональных стволовых клетках мыши (mESC) и клетках-предшественниках
олигодендроцитов (mOPC). Neat1 синтезируется с 19-й хромосомы, а Fgfr2 — c 7-й.
Источник: Nature Communication