Исследователи из Института теоретической и экспериментальной биофизики РАН (Пущино) раскрыли новый механизм действия широко известного препарата бетагистина, применяемого для улучшений микроциркуляции в сосудах. Оказалось, что он не только уменьшает симптомы головокружения, но и эффективно восстанавливает нейроны вестибулярных ядер мозга после повреждений, включая митохондрии — ключевые «энергостанции» клеток.
Открытие перспективно в разработке применения препарата при нейродегенеративных заболеваниях и ишемии. Результаты работы опубликованы в авторитетном журнале Neuroscience Letters.
Вестибулярные расстройства (чувство вращения, неустойчивость) затрагивают более трети людей старше 40 лет. Они возникают из-за дисфункции вестибулярных ядер в стволе мозга, в частности ядра Дейтерса (латеральное вестибулярное ядро). Эти нарушения также связывают с развитием нейродегенеративных заболеваний, таких как болезнь Альцгеймера и Паркинсона. Грамотное комбинирование препаратов при лечении пациента с головокружениями различной этиологии, в том числе являющихся симптомами нейродегенеративных нарушений, позволит ускорить восстановление вестибулярной функции со стабильным терапевтическим эффектом.
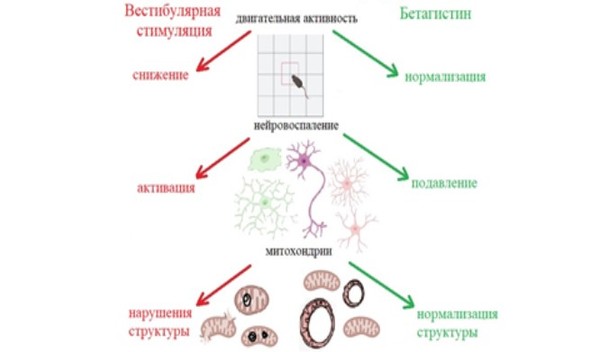
Применение препарата бетагистин восстанавливает митохондрии мозга, снижает нейровоспаление, нормализует поведенческие нарушения у мышей с индуцированной вестибулярной дисфункцией
Биофизики из Пущино исследовали действие применяемого от головокружения препарата (бетагистин) на животных и впервые показали его дополнительное нейропротекторное свойство. Исследование прокомментировала ведущий научный сотрудник лаборатории экспериментальной нейробиологии ИТЭБ РАН кандидат биологических наук Ирина Михеева: «В эксперименте мыши подвергались интенсивной вестибулярной стимуляции (длительному вращению), что вызывало у них стресс, нарушение координации и повреждение нейронов. Через час после стимуляции в нейронах ядра Дейтерса наблюдались характерные изменения: митохондрии набухали, теряли свою структуру, а внутри клеток появлялись митофагосомы — маркеры уничтожения повреждённых митохондрий. Препарат бетагистин перорально вводили животным после того, как повреждение уже произошло — через 1 час и через 24 часа после стимуляции. Результаты превзошли ожидания: у животных, получавших препарат, быстрее нормализовалась двигательная активность и исследовательское поведение в тесте „открытое поле”. Бетагистин подавлял реактивную активацию микроглии и астроцитов — клеток, вызывающих нейровоспаление. Через пять дней после стимуляции у леченых мышей уровень воспаления в ядре Дейтерса возвращался к норме, тогда как у нелеченых животных сохранялись его признаки. Препарат практически полностью устранял митофагосомы и способствовал появлению особых митохондрий в форме „пончика” (donut-shaped mitochondria). Считается, что такая форма помогает сохранять мембранный потенциал и защищает клетку от гибели».
Бетагистин давно используется в клинике для лечения болезни Меньера и вестибулярного головокружения, однако его нейропротекторные свойства долгое время оставались недооценёнными. Данное исследование впервые демонстрирует, что препарат эффективен при введении после повреждающего воздействия.
По словам авторов, бетагистин не только облегчает симптомы, но и запускает восстановительные процессы на клеточном уровне, включая нормализацию работы митохондрий и снижение нейровоспаления. Это открывает перспективы его применения при нейродегенеративных заболеваниях, ишемии и других состояниях, связанных с повреждением вестибулярной системы.
В дальнейшем авторы планируют исследовать нейропротекторные эффекты уридина и леветирацетама на модели вестибулярных нарушений. Каждый из этих препаратов обладает различным механизмом действия и точкой приложения. В рамках модели вестибулярных нарушений будет оценено их влияние на поведенческие реакции, а также на митохондриальные и нейрон-глиальные изменения, индуцированные вестибулярной стимуляцией.
Работа поддержана грантом Российского научного фонда (№25-25-00037).
Текст: Алсу Дюкина.
Источник: пресс-служба ИТЭБ РАН.