Группа учёных из Лаборатории
молекулярного дизайна и синтеза, Группы
экспрессии белковых факторов роста и дифференцировки ИБХ РАН,
Института полиомиелита и других институтов синтезировали серию соединений на
основе 5-(перилен-3-илэтинил)урацила и изучили их противовирусные свойства и
механизм действия. Предыдущие исследования данного класса соединений
предполагали противоречащие типы механизмов действия при сопоставимо высокой
активности. Настоящее исследование показало, что при облучении светом амфифильные
соединения, аккумулированные в клеточных и вирусных мембранах, ингибируют
проникновение в клетку оболочечных вирусов.
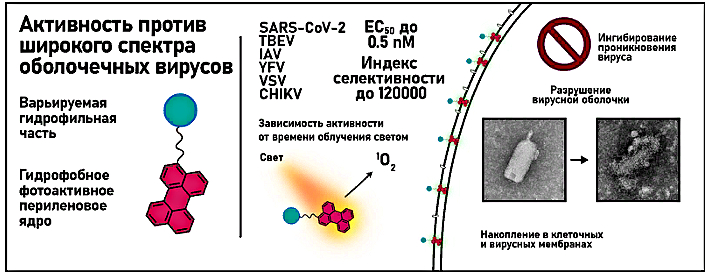
Рисунок 1. Графическое представление
полученных в работе результатов.
Амфипатические нуклеозидные и ненуклеозидные
производные пентациклического ароматического углеводорода перилена известны как
сильнодействующие нецитотоксические противовирусные средства широкого спектра
действия. В данной работе сообщается о
3-метил-5-(перилен-3-илэтинил)-урацил-1-уксусной кислоте и ее амидах, новой
серии соединений на основе 5-(перилен-3-илэтинил)-урацила. Соединения
демонстрируют выраженную активность in vitro в отношении переносимых
членистоногими вирусов, а именно вируса клещевого энцефалита (ВКЭ) и вируса
желтой лихорадки (ЖЛ), в анализах на уменьшение бляшек со значениями ЕС до 1,9
и 1,3 нМ соответственно, а также вируса чикунгунья (CHIKV) в тесте
ингибирования цитопатического эффекта со значениями ЕС до 3,2 мкМ. Соединения
были активны и в отношении респираторных вирусов: ингибировали коронавирус
(SARS-CoV-2), в тесте ингибирования цитопатического эффекта и вирус гриппа А
(IAV) в экспериментах по снижению титра вируса – значения ЕС до 51 нМ и 2,2 мкМ
соответственно (Рисунок 2).
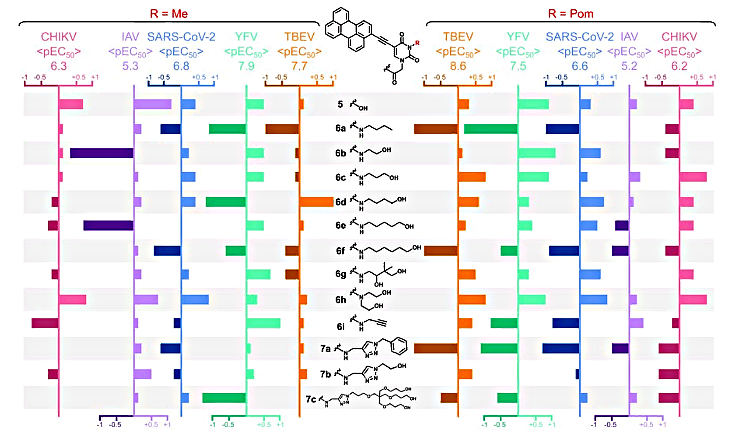
Рисунок 2. Диаграмма сравнения
активности. Каждая вертикальная ось соответствует средней противовирусной
активности среди N1-заместителей, среднее значение (pEC50 = -log10EC50)
отмечено над осью. Каждая полоса представляет собой отклонение активности (от
средней активности по вирусу) в зависимости от N1-заместителя. Каждая строка
соответствует одному N1-заместителю, в левой части приведены данные для ряда
N3-Me, в правом – для ряда N3-Pom. Отрицательные отклонения показаны
затемненными полосами.
Активность определяется наличием гидрофобного
периленового ядра (Рисунок 1), все синтезированные соединения показали
сопоставимые скорости генерации синглетного кислорода 1О2.
Тем не менее активность может варьироваться на порядки в зависимости от
гидрофильной части молекулы, что указывает на сложный механизм действия
(Рисунок 2).
Эксперимент по времени добавления и флуоресцентная
визуализация показывают, что соединения ингибируют проникновение вирусов в
клетки. Локализация соединения в липидных бислоях и видимое повреждение
вирусной оболочки предполагают мембрану в качестве первичной мишени. Резкое
снижение противовирусной активности при ограниченном доступе света или при
добавлении антиоксидантов подтверждает идею о фотоиндуцированном
АФК-опосредованном повреждении вирусной оболочки как способе противовирусного
действия.
Исследование опубликовано в журнале Antiviral Research.
Источник: ИБХ РАН.